时间:2022-02-24 15:13
病毒是基因治疗的天生载体
最近大家肯定常被工具病毒介导的基因治疗刷屏。
有研究者认为,病毒是天生的载体。相较于容易污染的细胞、转导效率低的非病毒载体,工具病毒有着出彩的效果。据 2017 年的统计,迄今为止大约三分之二的基因治疗试验使用病毒载体。
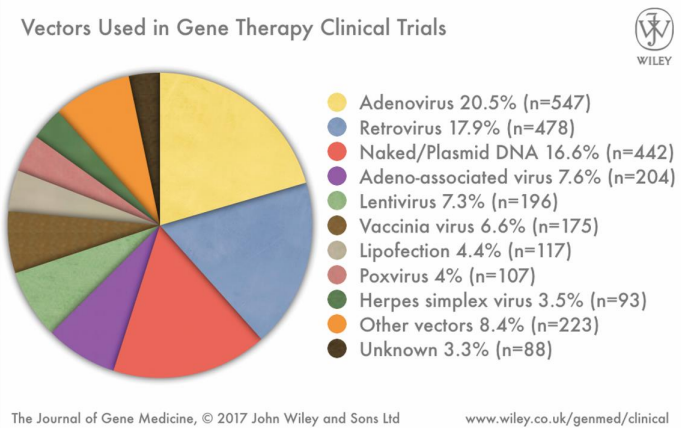
(图源:doi.org/10.1002/jgm.3015)
AAV是首选
腺相关病毒(AAV)介导的基因治疗已经成为某些遗传性疾病的首选治疗方法。2012年欧盟第一次批准基于AAV的药物Glybera治疗蛋白脂肪酶缺乏症,2018年美国第一次批准AAV药物用于治疗先天性失明(遗传性视网膜营养不良)。
AAV也有弱点
尽管,AAV病毒载体可能是最有效的基因治疗载体,但AAV有限的荷载能力使其应用受到了大大的限制。AAV病毒载体装载的DNA序列长度不超过5kb,而且这还要包括一些调控元件,因此AAV病毒载体对于一些较大的基因就无能为力了,这也限制了基因疗法在递送大基因上的应用。
Delivery!Delivery!
为了克服这种限制,已探索了多种策略。
其一是将大的转基因分割开来,通过2个或3个AAV运输到靶标。其二是促进单个AAV载体传递超大基因。
下面我们将以这两种策略为基础,讨论AAV运输超大基因的可能性。
策略1:拆分超大基因组表达框
我们可以将超大的基因表达框分开,分成两个或三个部分,再由两个或三个单独的AAV载体携带。同时向靶细胞传递后,在细胞内重组整个大基因表达框,表达完整的大蛋白。
根据重组机制的不同,可将拆分表达框的方法分为:反式剪接、重叠、杂交和三重AAV载体。
Trans-splicing AAV Vectors
反式剪接AAV载体利用了AAV固有的聚合,通过ITR介导的分子间重组,如下图所示。到目前为止,这种方法已成功地用于血管性血友病von Willebrand因子、Stargardt疾病ATP结合框4、1B型Usher综合征肌球蛋白VIA及血友病A的作用因子VIII的传递。
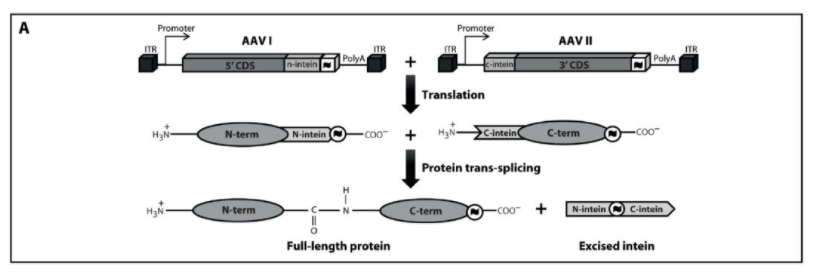
Overlapping AAV Vectors
重叠AAV载体利用编码序列中的同源重组来重建一个大的基因表达框。其中一个AAV载体包含启动子和编码序列的5’部分,而另一个AAV载体携带编码序列和polyA信号的3’部分。这两个AAV载体中的编码序列共享一个同源区域,并依次诱导靶细胞中大蛋白的表达。
同时,重叠AAV载体的效率在很大程度上依赖于编码序列重叠区域的同源重组。
Hybird AAV Vectors
杂交AAV载体结合了反式剪接和重叠AAV载体的机制。与反式剪接载体相比,杂交载体中重叠区域的同源重组效率更高,大大增加了成对载体的方向正确性。这种方案已成功地用于传递大的治疗基因,包括CFTR、ABCA4 and MYO7A和Dysferlin等。
Triple AAV Vectors
双病毒策略可将AAV包装容量扩充到10kb,但对于一些巨大的基因转移仍是不够的,基于三病毒的策略应运而生。这些载体被设计成转移多达15kb的遗传物质。例如,利用混合ITRs和反式剪接的三重AAV载体成功地诱导了营养不良肌肉中全长11kb的营养不良蛋白基因的表达;利用反式剪接和杂交三重AAV载体,全长的CDH23和ALMS1成功在视网膜中表达。
但是目前这种方案的转导效率较低。
总的来说,以上策略均有较大的发展潜力。但值得注意的是,双重或三重载体共同传递,不可避免地增加了使用载体的剂量。高剂量AAV给药不可避免地产生严重的毒性,因此“在低剂量下载体高效率转导”至关重要。
策略2:将超大基因组塞进单个AAV
单个AAV载体传递大型表达框的策略应运而生。
Fragmented Oversized AAV Gene Delivery
在包装超大基因组时,达到最大包装容量或遇到终止信号时包装即会停止,从而产生不同大小的异质片段基因组。当含这些片段的AAV载体传递到靶细胞时,片段基因组的同源重组恢复表达框并介导大蛋白的表达。
大体上,这种片段化基因传递方式效率低于完整基因传递。然而,在某些情况下,单个AAV片段基因传递比多重AAV载体更有效。例如,在肌肉和视网膜中,片段AAV载体比反式剪切AAV载体诱导更强的荧光素酶表达(PMID: 23939025)。在传递另一个大基因MYO7A时,重叠AAV载体的表达明显低于单个AAV片段基因传递(PMID: 23344065)。
因此,单个AAV片段基因传递一种可行的替代方案。
Other strategies
还有几种额外的策略帮助单个AAV载体传递超大基因组,包括衣壳改造、改善病毒产生、给药蛋白酶体抑制剂、优化转录元件等。
比如,VP2衣壳蛋白的缺失可以将AAV载体的包装能力提高到6kb(PMID: 16014954),采用HBoV1衣壳蛋白的AAV成功地包装了CFTR基因组(PMID: 23896725),在过大的AAV. VIII传递时给予蛋白酶体抑制剂可将Factor VIII的表达增强三到六倍(PMID: 20700109)。
AAV介导的多转基因传递
除了单个超大基因组的传递,多个基因组的传递问题也值得探讨。
这其中可以选择多种策略,如将多个片段塞入同一个AAV载体,或同时传递两个甚至三个AAV载体。
Single AAV Vectors
如果两个转基因的大小在5kb的包装限制内,这两个转基因的编码序列可以被设计成一个AAV载体。
Co-delivery of Two or Three AAV Vectors
如果两个转基因均大于5kb,则可以使用两个携带不同完整基因表达框的AAV载体。既往研究证实,两个携带不同报告基因的AAV载体可以调节这两个蛋白在肌肉[PMID: 15353044]、视网膜和海马[PMID: 22545762]的同一细胞中的表达。
同样,使用三个AAV载体分别表达三个基因的情况。在Shen等人[PMID: 10945765]和Muramatsu等人[PMID: 11860702]的研究中,通过三个AAV载体分别表达了TH、AADC和GCH基因,改善了帕金森小鼠模型的疾病表型。
总结
随着临床试验的日益成功,AAV基因治疗将扩展到更多的疾病。多种应用策略的探索也为解决AAV包装容量限制问题提供了方案。一些传递超大基因的策略已经取得了显著成效进展。随着我们不断努力开发和调整AAV载体,毫无疑问AAV基因治疗将有助于治疗更多的疾病。
布林凯斯现提供上述内容相关AAV过表达/干扰服务!
可以联系我们了解详情哦~
本文未经授权禁止转载
如有需要,可联系小编获取原文
