简介
狂犬病毒(Rabies Virus,RV)属于弹状病毒科(Rhabdoviridae)狂犬病毒属(Lyssavirus),其基因组是长约12 kb的单股负链RNA,由3′端至5′端依次排列着N、P、M、G和L共5个狂犬病毒的结构基因,分别编码核蛋白、磷蛋白、基质蛋白、糖蛋白和转录酶大蛋白(如图1 )。
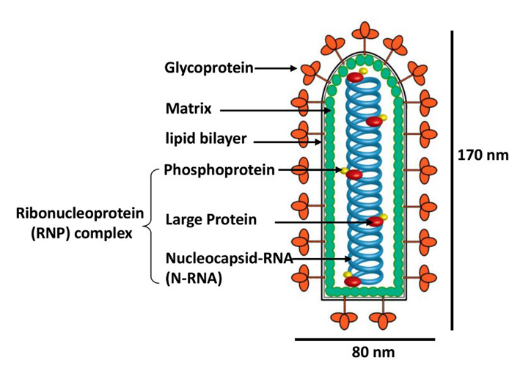
图1. RV粒子示意图(图片来自whelanlab网站)
RV在宿主体内,病毒糖蛋白G介导病毒粒子与细胞表面受体结合,通过内吞作用进入细胞。随后通过pH介导膜融合,促使RV基因组释放到细胞质中。感染病毒粒子内包装的L、N、P共同构成的聚合酶复合物以基因组负链RNA为模板启动转录表达,复制,组装,出芽产生子代病毒。(如图2)
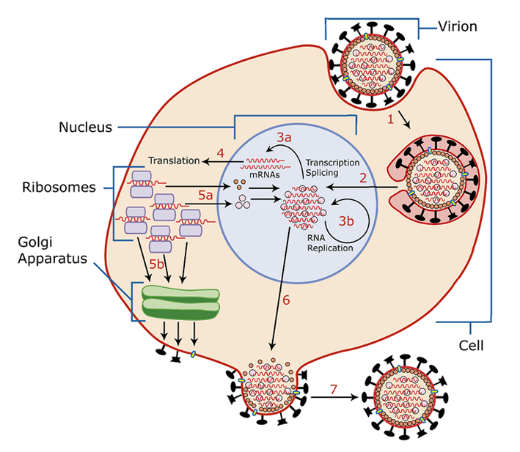
图2. 狂犬病毒生命周期示意图(图片来自维基百科)
野生型RV是人畜共患的狂犬病的致病因子,在神经系统中具有传播属性,对人和动物均具有较高致病性。因此本公司RV产品以狂犬病毒疫苗株(SAD B19或CVS-N2c)且缺失G蛋白的复制缺陷型RV (RV-SAD-ΔG/ RV-CVS-ΔG) 为骨架改造而来。随着反向遗传学手段的成熟,经过改造的RV,可用于神经回路研究。RV感染中枢系统后,主要标记神经元,几乎不标记胶质细胞;被感染的神经元在一定时间内(7-12天)几乎不发生明显病变及裂解。目前RV系统可分为逆向标记系统和逆向跨单突触系统。
第一代逆向标记系统(RV-SAD-B19G-ΔG)
RV的囊膜糖蛋白(glycoprotein,G)是其逆行跨突触所必需的蛋白,G蛋白缺失的RV(RV-SAD-ΔG)会丧失跨突触能力,但其复制及转录不受影响(可持续高丰度表达外源基因),因此,包裹SAD B19G蛋白的RV(RV-SAD-B19G-ΔG)携带报告基因后,可逆向高亮度标记神经元精细形态。
第二代逆向标记系统(RV-CVS-N2C(G)-ΔG)
第二代逆向标记系统采用CVS-N2c毒株,它具有更低的神经毒性以及更强的跨突触突触传递能力,第二代逆向标记RV-CVS-N2C(G)-ΔG产品能在相同滴度达到比第一代RV-SAD-B19G-ΔG更好的逆向标记效果,且神经毒性更低。
 图3. RV-CVS-N2c-ΔG-EGFP(布林凯斯测试)
图3. RV-CVS-N2c-ΔG-EGFP(布林凯斯测试)
第一代逆向跨单突触系统(RV-SAD-EnvA-ΔG)
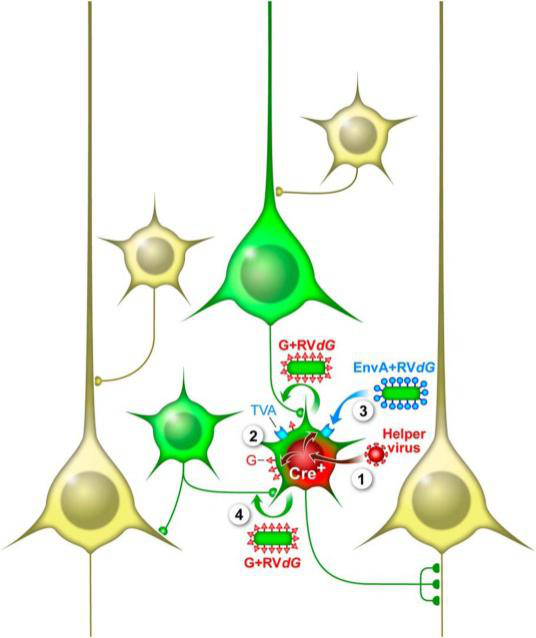
利用重组的禽类肉瘤病毒(Aviansarcoma-leukosisvirus,ASLV)的外膜蛋白(EnvA)融合蛋白包装RV-SAD-ΔG基因组形成的病毒粒子(RV-SAD-EnvA-ΔG),可特异性识别EnvA的受体TVA(TVA只存在于禽类细胞中,在哺乳动物神经元中无表达)介导病毒特异性地感染细胞。利用Cre转基因鼠结合Cre-LoxP控制表达TVA及G蛋白的AAV辅助病毒(DIO-TVA和DIO-RVG),可实现只在特定区域特异类型神经元中表达TVA及G蛋白,从而利用RV-SAD-EnvA-ΔG实现对特异类型神经元的逆向跨单级突触标记(如图3)。在此基础上,使RV-SAD-EnvA-ΔG带上ChR2及GCaMP等基因,可实现对特异类型神经元的直接输出 网络进行功能操纵及活动监测。
图4. RV-SAD-EnvA-ΔG实现神经元的逆向跨单级突触标记(Callaway, et al., The Journal of neuroscience: the official journal of the Society for Neuroscience, 2015)
第二代逆向跨单突触系统(RV-CVS-EnvA-ΔG)
第二代逆向跨单突触系统采用CVS-N2c毒株,利用Cre转基因鼠结合Cre-LoxP控制表达TVA及G蛋白的AAV辅助病毒(DIO-TVA 和DIO-N2cG),可实现只在特定区域特异类型神经元中表达TVA及G蛋白,从而利用RV-EnvA-ΔG实现对特异类型神经元的逆向跨单级突触标记(原理同第一代逆向跨单突触系统)。RV-CVS-EnvA-ΔG与第一代逆向跨单突触系统比较,它具有更低的神经毒性以及更强的跨突触突触传递能力。
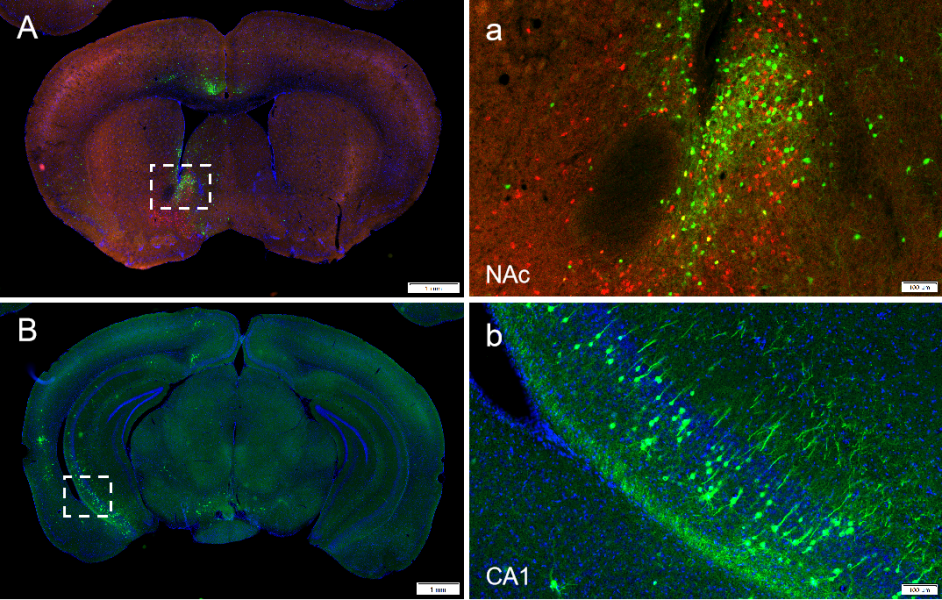 图5. RV-CVS-EnvA-ΔG-EGFP(布林凯斯测试)
图5. RV-CVS-EnvA-ΔG-EGFP(布林凯斯测试)
应用
1)特定区域特异类型神经元的全脑单级输入网络标记;(见案例展示二)
2)两个区域特异类型神经元跨单级输入网络标记;(见案例展示一)
3)三级连接网络的跨单突触标记。
4)携带ChR2或GCaMP的RV应用
产品列表
布林凯斯RV系列产品分为RV-CVS株和SAD-B19疫苗株。
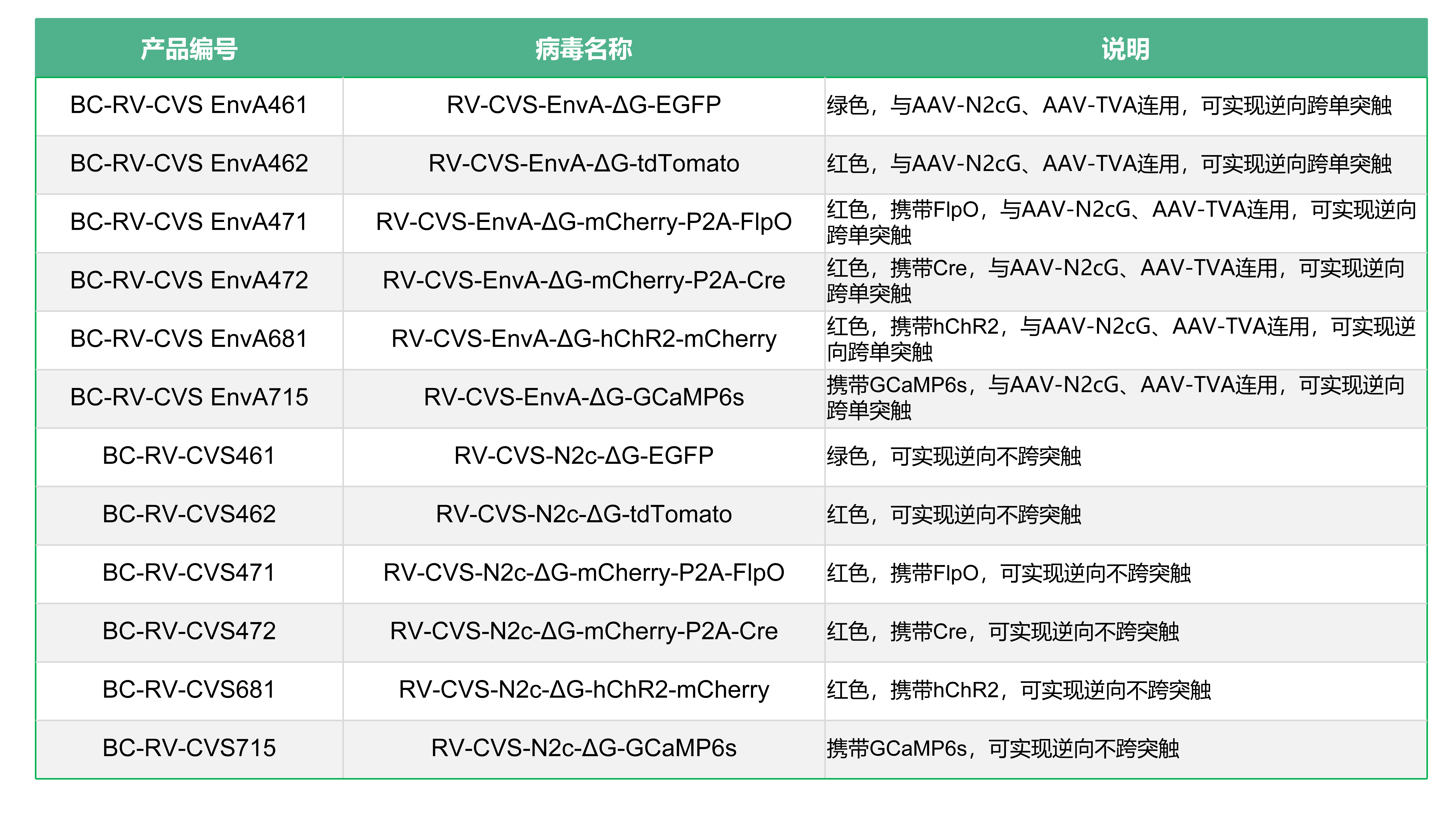
RV-CVS株产品列表:
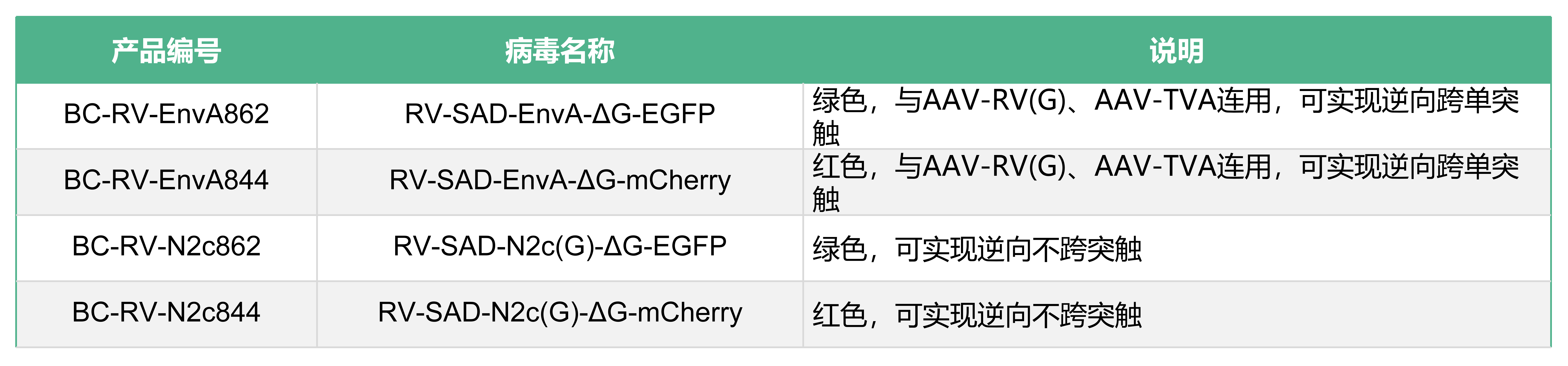
SAD-B19株产品列表:
案例展示
实例一:逆向标记海马锥体神经元中同时作用于mPFC和ACB中的GABA能神经元(图6,PMID: 31285615)
实验动物:抑制性神经元(SST, PV, VIP)的Cre小鼠
使用的病毒:RV-EnvA-GFP,AAV-DIO-TVA-hBFP和AAV-DIO-RG
实验方法和结果:在抑制性神经元(SST, PV, VIP)的Cre小鼠mPFC脑区注射RV-EnvA-GFP以及Cre依赖的辅助病毒AAV-DIO-TVA-hBFP和AAV-DIO-RG实现逆向跨单级突触,同时在ACB脑区注射从轴突末梢吸收的RV-DG-DsRed,病毒逆向标记海马体投射到ACB区的神经元,最终找到海马体中同时调控mPFC和ACB区的GABA能神经元。(如图6)
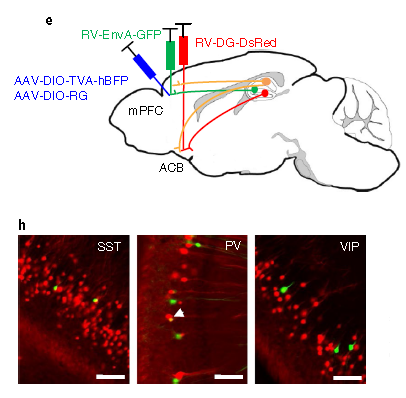
图6. 标记海马锥体神经元中同时作用于mPFC和ACB中的GABA能神经元
实例二:VTA多巴胺能神经元分离的支配NAC和mOT(图7,PMID: 29251597)
实验动物:C57BL/6 mice
使用的病毒:RV-DG-DsRed和RV-DG-GFP,滴度10的8次方TU
实验方法和结果:分别注入100 nl RV-DG-DsRed和RV-DG-GFP在NAC和mOT中,1周后灌流取材,可在VTA追踪到神经元。(如图7)
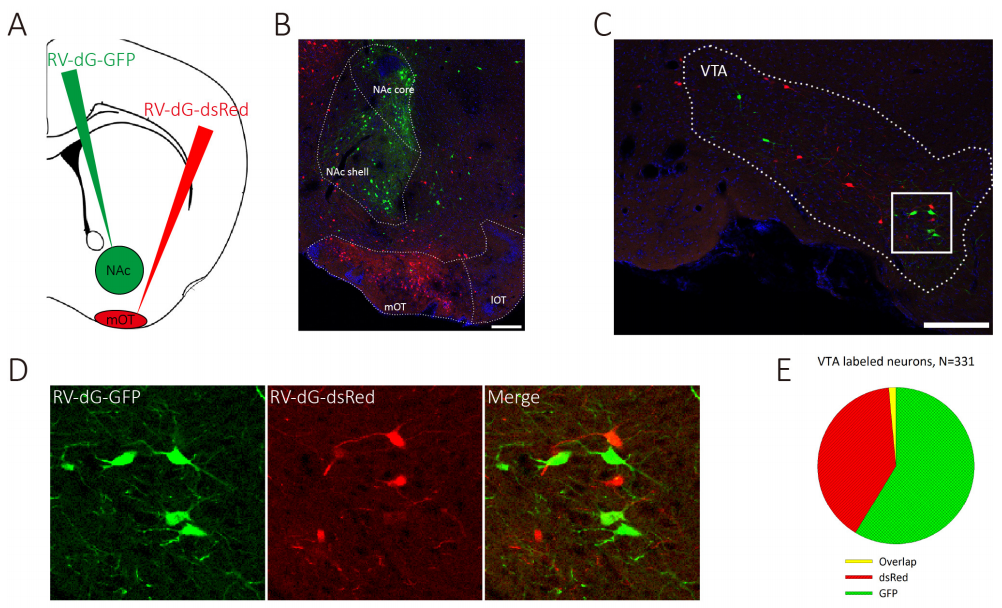
图7. VTA多巴胺能神经元分离的支配NAC和mOT