时间:2020-09-08 15:31

2020年7月,斯坦福大学Thomas R. Clandinin团队报道了一种基于Gal4-UAS表达系统的稀疏标记技术,该技术通过构建一种双稳态的重组酶依赖性遗传竞争环境,实现对单个细胞亚群的标记和操纵。
No.1---Gal4-UAS双元表达体系的构建
Gal4 和UAS 都是与酵母半乳糖代谢调控相关的调控因子。其中GAL4是转录调控因子,其转录结合域(BD)与UAS(upstream activating sequence,增强子)序列结合,激活域(AD)和启动子序列结合,从而诱导基因的表达。早在1988 年,Fischer 研究组发现在果蝇中表达Gal4 并不影响其正常生长和发育,并且组织特异性表达的Gal4 能以激活UAS 及其融合的下游目的基因的转录。基于以上Gal4-UAS系统双元表达策略,构建了3个果蝇转基因体系:

图:Gal4-UAS表达系统
(1):构建并鉴定出特定神经元及其亚群(如视神经叶包括Mi1、T4、T5、HS等神经元亚群)中表达Gal4的转基因系果蝇;
(2):构建nSyb(神经元小突触泡蛋白)启动子的调控之下的PhiC31重组酶质粒nSyb-PhiC31,注射到果蝇胚胎细胞中,利用In-Fusion cloning技术介导位点特异性同源重组构建并筛选PhiC31转基因果蝇系,实现广泛的特异性神经元高效率表达。
-----PhiC31,一种能识别噬菌体attP位点和细菌attB位点并介导位点之间进行不可逆、高效整合的重组酶,作用于噬菌体感染细菌之后溶源的态建立。
(3):构建UAS-attp-attb-效应子的质粒载体(文中简称SPARC),并利用CRISPR-HDR技术,将该质粒DNA结合gRNA导入到果蝇基因组特定位点诱发双键断裂后的同源重组修复,实现SPARC的delivery.
No.2---SPARC双稳态表达架构的建立
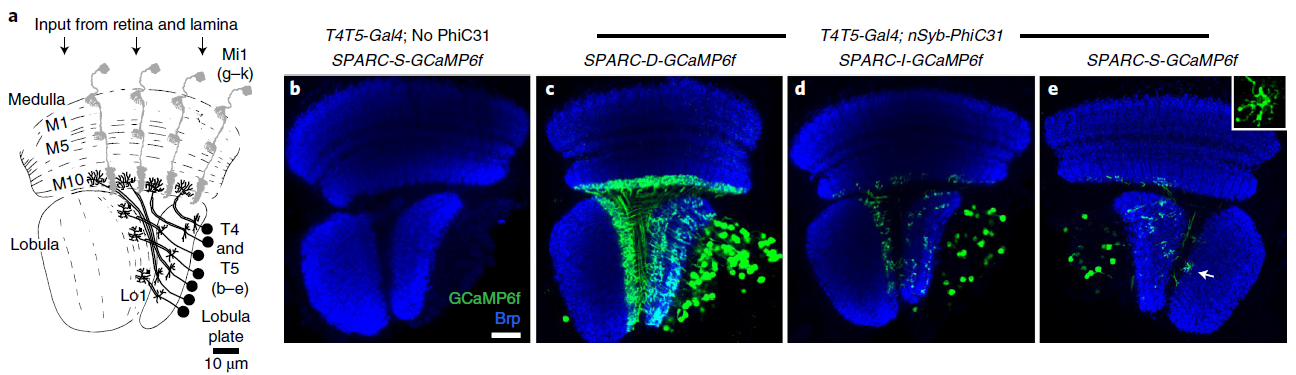
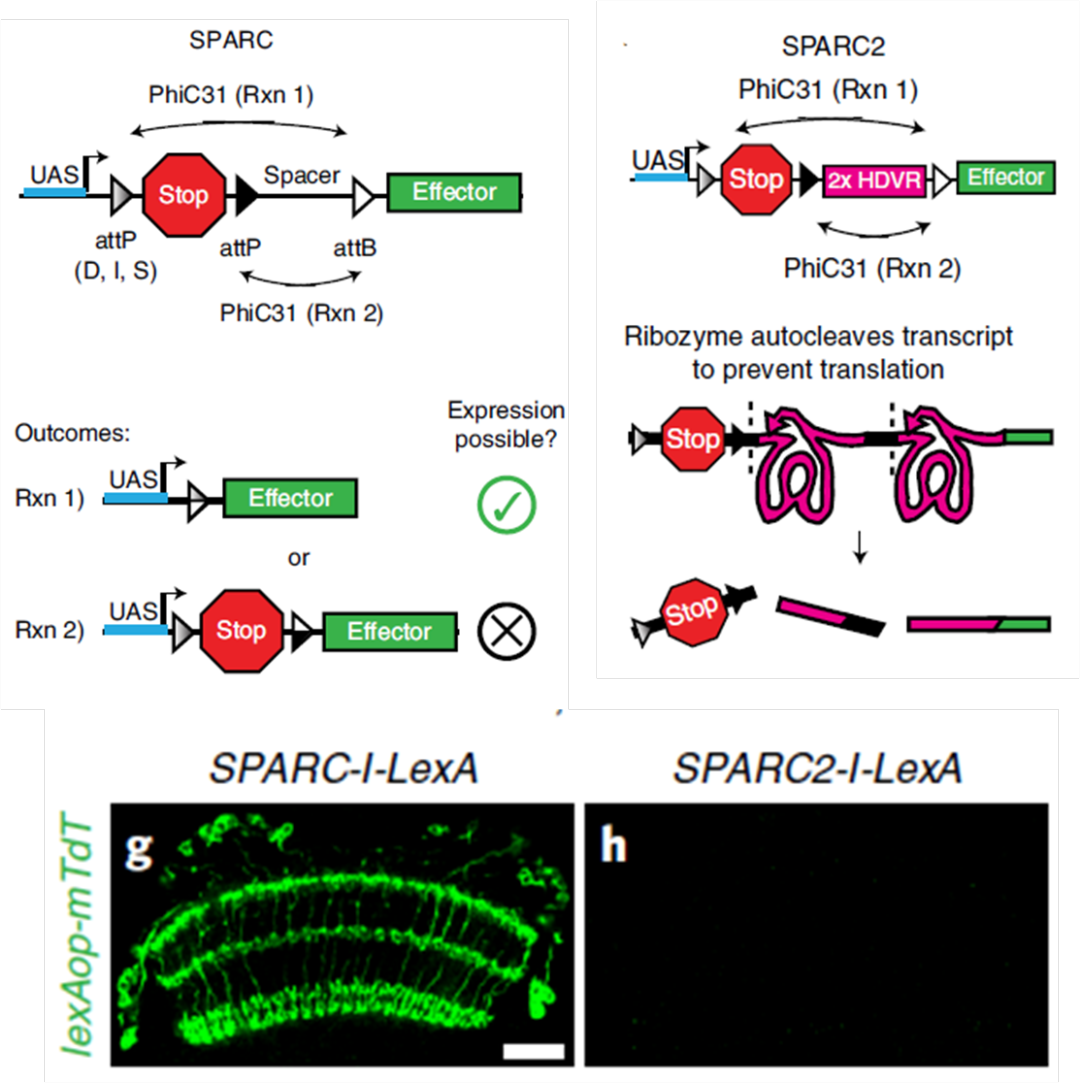
接下来,本文研究者设计了SPARC的基本架构:其中PhiC31通过颠倒效应子GCaMP6f编码序列的方向,在GCaMP6f两侧加入了标准的attP和attB序列,使其能够在Gal4驱动下表达;另外,他们还设置了一系列attP突变对照组,分别将attP截断为34个碱基对(bp)的序列(34bp_attP-S)、38bp_attP-I以及60bp_attP-D,其中34bp_attP-S在大肠杆菌中经测试只有7%介导重组。

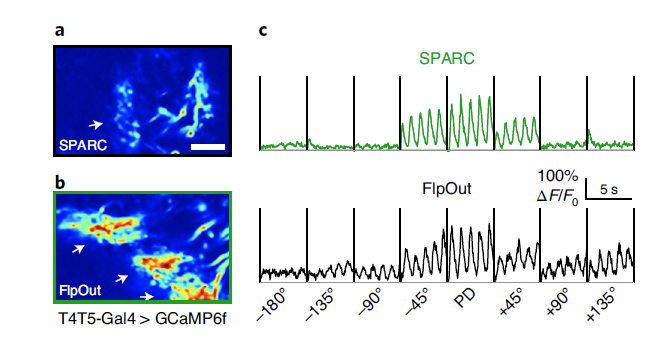
为了研究SPARC的功能效用,作者使用SPARC-S-GCaMP6f对单个T5神经元树突进行钙成像。不同于FlopOut方法,需要对果蝇幼虫进行滴定和精确的热休克处理,SPARC可将效应子的表达限制在细胞的亚群上,同时始终标记更少的T5神经元。由于每个T5神经元的树突位置特别接近,并且方向具有不同的选择性,所以单个细胞的稀疏标记对于功能的研究具有重要的意义。
【参考文献】
1,Jesse Isaacman-Beck et al,. SPARC enables genetic manipulation of precise proportions of cells. Nature Neuroscience volume 23, pages1168–1175(2020)
2,Roumen Voutev and E. Jane Albert Hubbard. A “FLP-Out” System for Controlled Gene Expression in Caenorhabditis elegans. Genetics September 1, 2008 vol. 180 no. 1 103-119
3,Dionne, H., Hibbard, K. L., Cavallaro, A., Kao, J.-C. & Rubin, G. M. Genetic reagents for making split-GAL4 lines in Drosophila. Genetics 209, 31–35 (2018).
4,Thorpe, H. M. & Smith, M. C. In vitro site-specific integration of bacteriophage DNA catalyzed by a recombinase of the resolvase/invertase family. Proc. Natl Acad. Sci. USA 95, 5505–5510 (1998).
5,Fischer JA, Giniger E, Maniatis T, Ptashne M. 1988. GAL4 activates transcription in Drosophila. Nature 332:853–856.
神经科学研究就找布林凯斯!
感兴趣的话快来联系我们吧~
本文未经授权禁止转载
如有需要,可联系小编获取原文